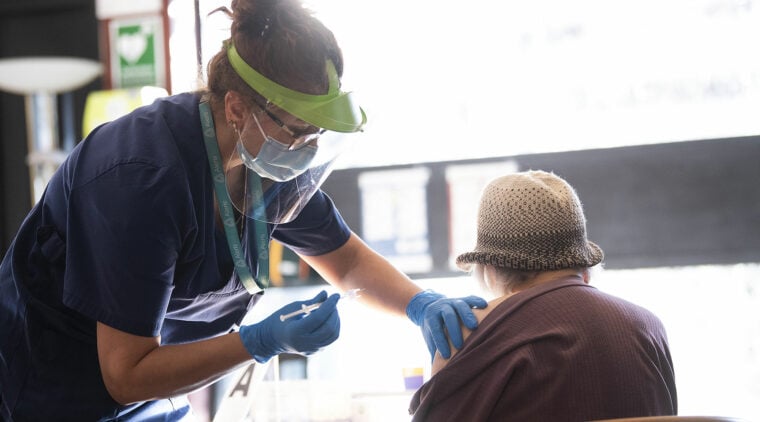
I dag tisdag meddelade att Sverige i likhet med en rad andra europeiska länder pausar Astra Zenecas coronavaccin.
– Det är en normal följd av att man på grund av att så många fått vaccinet får en mer specificerad bild av biverkningarna. I detta fall har man upptäckt en misstänkt ökning av en särskild typ av blodproppar, kombinerat med blödningar hos personer som fått vaccinet, säger Agnes Wold, professor och överläkare vid Göteborgs universitet.
– Det är en typ av blodpropp som normalt är extremt ovanlig – några fall per miljon personer och är inte den ”vanliga” blodproppen som drabbar många äldre personer.
Att beslutet är en försiktighetsåtgärd i väntan på att den europeiska läkemedelsmyndigheten EMA utreder de specifika fallen, betonade också statsepidemiolog Anders Tegnell när beskedet om pausen kom i på tisdagsmorgonen: Hittills har man inte sett ett tydligt orsakssamband mellan vaccinet och händelserna och inget misstänkt fall har rapporterats i Sverige.
Enligt Agnes Wold är pausen en illustration av hur utvärderingar av nya läkemedel, inklusive vaccin brukar gå till:
– Normalt börjar man med så kallade Fas 1-studier och testar vaccinet på ett fåtal friska frivilliga försökspersoner för att se att det inte är farligt.
Därefter följer Fas 2-studier, som också utförs på en liten homogen grupp patienter för att bekräfta att vaccinet är säkert, testa olika doser och se om man får ett immunsvar.
– Försökspersonerna har ofta väldigt likartad sjukdom och får inte äta andra läkemedel. I denna grupp ingår både män och kvinnor, säger Agner Wold. I Fas 3-studier utsätts försökspersonerna för smitta, normalt under naturliga förhållanden, att man smittas av den sjukdom som finns i samhället, i vissa fall genom att man medvetet smittar dem). Försökspersonerna lottas till att få riktigt vaccin eller placebo, som brukar vara en spruta med koksalt.
– Fas 3-studier brukar göras på några tusen personer i varje grupp, men med covidvaccinerna har man haft jättestora grupper, 10000-20000 i vaccin- respektive placebogrupp. Sedan jämför man hur många som blivit sjuka i respektive grupp och räknar ut hur bra skydd mot sjukdomen som vaccinet ger. Man noterar alla symtom och sjukdomar i grupperna för att se om något är vanligare i vaccingruppen, då är det en biverkan.
Det är efter fas 3 som läkemedelsföretaget kan ansöka om att deras preparat ska bli godkänt.
– Man känner då till alla typer av biverkningar som är någotsånär vanliga. Sen, när vaccinet är ute, fortsätter så kallade fas 4-studier, som man kan kalla en regulatorisk fas. När vaccinet getts till miljontals människor kan mycket ovanliga symtom eller sjukdomar dyka upp hos dem som fått vaccinet. Man måste då undersöka om de är vanligare än i befolkningen i samma ålder, för det är bara då man kan tala om en biverkan.
– I det här fallet har man pausat för att närmare få en bild av om det är en biverkan av vaccinet, och vad man i så fall ska göra, säger Agnes Wold.
Regeringens vaccinsamordnare Richard Bergström sa på tisdagen att han hoppas att man kan lämna besked om vaccinet redan på torsdag. Då ska EMA:s säkerhetskommitté PRAC, där EU-ländernas läkemedelsverk ingår, ha möte om den fortsatta vaccineringen med Astra Zenecas –
– De sammanträder på torsdag. Det blir intressant att veta vad de kommer fram till. Men det blir några dagars stopp minst, sa Richard Bergström.
Omkring 17 miljoner människor i EU och Storbritannien har injicerats med Astra Zenecas vaccin, uppgav företagets medicinska chef Ann Taylor i ett pressmeddelande på tisdagen.
– Det är en normal följd av att man på grund av att så många fått vaccinet får en mer specificerad bild av biverkningarna. I detta fall har man upptäckt en misstänkt ökning av en särskild typ av blodproppar, kombinerat med blödningar hos personer som fått vaccinet, säger Agnes Wold, professor och överläkare vid Göteborgs universitet.
– Det är en typ av blodpropp som normalt är extremt ovanlig – några fall per miljon personer och är inte den ”vanliga” blodproppen som drabbar många äldre personer.
Att beslutet är en försiktighetsåtgärd i väntan på att den europeiska läkemedelsmyndigheten EMA utreder de specifika fallen, betonade också statsepidemiolog Anders Tegnell när beskedet om pausen kom i på tisdagsmorgonen: Hittills har man inte sett ett tydligt orsakssamband mellan vaccinet och händelserna och inget misstänkt fall har rapporterats i Sverige.
Enligt Agnes Wold är pausen en illustration av hur utvärderingar av nya läkemedel, inklusive vaccin brukar gå till:
– Normalt börjar man med så kallade Fas 1-studier och testar vaccinet på ett fåtal friska frivilliga försökspersoner för att se att det inte är farligt.
Därefter följer Fas 2-studier, som också utförs på en liten homogen grupp patienter för att bekräfta att vaccinet är säkert, testa olika doser och se om man får ett immunsvar.
– Försökspersonerna har ofta väldigt likartad sjukdom och får inte äta andra läkemedel. I denna grupp ingår både män och kvinnor, säger Agner Wold. I Fas 3-studier utsätts försökspersonerna för smitta, normalt under naturliga förhållanden, att man smittas av den sjukdom som finns i samhället, i vissa fall genom att man medvetet smittar dem). Försökspersonerna lottas till att få riktigt vaccin eller placebo, som brukar vara en spruta med koksalt.
– Fas 3-studier brukar göras på några tusen personer i varje grupp, men med covidvaccinerna har man haft jättestora grupper, 10000-20000 i vaccin- respektive placebogrupp. Sedan jämför man hur många som blivit sjuka i respektive grupp och räknar ut hur bra skydd mot sjukdomen som vaccinet ger. Man noterar alla symtom och sjukdomar i grupperna för att se om något är vanligare i vaccingruppen, då är det en biverkan.
Det är efter fas 3 som läkemedelsföretaget kan ansöka om att deras preparat ska bli godkänt.
– Man känner då till alla typer av biverkningar som är någotsånär vanliga. Sen, när vaccinet är ute, fortsätter så kallade fas 4-studier, som man kan kalla en regulatorisk fas. När vaccinet getts till miljontals människor kan mycket ovanliga symtom eller sjukdomar dyka upp hos dem som fått vaccinet. Man måste då undersöka om de är vanligare än i befolkningen i samma ålder, för det är bara då man kan tala om en biverkan.
– I det här fallet har man pausat för att närmare få en bild av om det är en biverkan av vaccinet, och vad man i så fall ska göra, säger Agnes Wold.
Regeringens vaccinsamordnare Richard Bergström sa på tisdagen att han hoppas att man kan lämna besked om vaccinet redan på torsdag. Då ska EMA:s säkerhetskommitté PRAC, där EU-ländernas läkemedelsverk ingår, ha möte om den fortsatta vaccineringen med Astra Zenecas –
– De sammanträder på torsdag. Det blir intressant att veta vad de kommer fram till. Men det blir några dagars stopp minst, sa Richard Bergström.
Omkring 17 miljoner människor i EU och Storbritannien har injicerats med Astra Zenecas vaccin, uppgav företagets medicinska chef Ann Taylor i ett pressmeddelande på tisdagen.